近日我所畜禽重要人兽共患病团队在国际免疫学杂志《Frontiers in Immunology》在线发表了题为“The cGas–Sting Signaling Pathway Is Required for the Innate Immune Response Against Ectromelia Virus”的研究论文(论文链接https://www.frontiersin.org/articles/10.3389/fimmu.2018.01297/full)。文章首次报道了cGAS-STING信号通路在抵抗ECTV感染的抗病毒天然免疫反应中扮演了重要的角色。
天然免疫是宿主抵抗病原微生物入侵的第一道防线。cGAS是宿主最关键的DNA识别受体,能激活STING-TBK1-IRF3信号轴诱导Ⅰ型IFNs的产生,进而介导机体的抗病毒天然免疫反应。因此,cGAS被认为是宿主“真正的”胞质DNA识别受体。ECTV感染小鼠能引起鼠痘,是实验小鼠、大鼠和豚鼠等的一种高度接触性传染病。ECTV属于痘病毒科正痘病毒属,与天花病毒、猴痘病毒和牛痘病毒等人兽共患痘病毒的亲缘关系较近,但其宿主范围较窄,只感染鼠类,而其它正痘病毒却能同时感染人类和多种动物。因此,ECTV不仅是天花病毒、猴痘病毒等人兽共患痘病毒跨种感染与传播研究的良好替代模型,也是痘病毒与宿主天然免疫互作机制研究的良好模型。
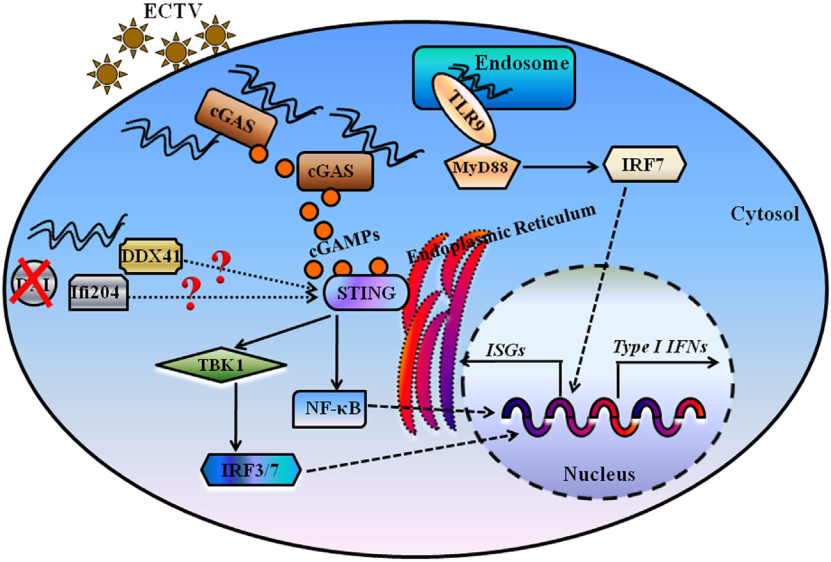
该研究基于基因芯片转录组学分析发现,鼠痘病毒感染小鼠后cGAS-STING信号通路及相关分子出现了显著性的上调表达。然后采用双荧光素酶报告系统发现,cGAS和STING都具有启动ECTV诱导IFN-β高表达的能力;同时通过过表达和敲降试验证实,ECTV感染细胞后通过cGAS和STING显著诱导IFN-β的表达以及TBK1和IRF3的磷酸化。利用基因敲除细胞证实,cGAS-STING-TBK1-IRF3信号通路参与了ECTV诱导IFN-β的产生,且cGAS和STING具有限制ECTV增殖的能力。通过基因敲除小鼠的体内试验,进一步确认cGAS-STING信号转导通路在拮抗ECTV感染中所发挥的至关重要的作用(见下图)。本研究首次从细胞与动物个体水平阐明了cGAS-STING-TBK1-IRF3信号轴对ECTV感染的抗病毒天然免疫反应的分子作用机制,为揭示人兽共患痘病毒感染宿主的抗病毒天然免疫反应的分子机制奠定理论基础。
畜禽重要人兽共患病团队的2014级博士生成温玉和助理研究员何小兵是本文的共同第一作者,景志忠研究员为该论文的通讯作者。该研究得到了甘肃省自然科学基金青年项目(17JR5RA325)、兰州兽医研究所科研基本业务费专项(1610312016019)、中国农业科学院基本科研业务费专项(1610312017005)和国家自然科学基金青年项目(31302072)的资助。此外,这也是该团队完全利用自己建立的研究平台,通过院创新工程取得的研究进展。(畜禽重要人兽共患病团队/科技处)