近日,中国农业科学院兰州兽医研究所口蹄疫与新发病流行病学团队解析了小RNA病毒VP3通过TP53-BAD-BAX轴诱导自噬促进病毒复制增强致病性的作用机制。相关研究结果以“Picornavirus VP3 protein induces autophagy through the TP53-BAD-BAX axis to promote viral replication”为题,发表于《自噬》(Autophagy)。
小RNA病毒能够在人类和动物中引起不同传染性疾病,其进化出多种策略来操纵细胞自噬和凋亡以促进病毒复制和致病,但宿主细胞凋亡和自噬影响病毒复制和致病的机制尚不清楚。该研究发现口蹄疫病毒(FMDV)、脊髓灰质炎病毒(PV)和塞内卡病毒A(SVA)的结构蛋白VP3是病毒复制和致病过程中的关键毒力因子,能够诱导细胞自噬和凋亡。该研究利用FMDV作为模型,深入探究了这些病毒如何操纵细胞机制促进病毒复制和致病。研究结果显示,FMDV的VP3蛋白直接与TP53蛋白相互作用,增强TP53的磷酸化,促进其转移到线粒体,并增强TP53与BAD的相互作用,进而诱导自噬和凋亡反应。VP3诱导的自噬和凋亡对FMDV复制至关重要,但自噬在VP3介导的致病机制中发挥主导作用。VP3蛋白上的甘氨酸129位点(Gly129)被鉴定为诱导凋亡和自噬的关键位点。通过构建突变重组毒,发现在FMDV感染过程中,Gly129不仅对VP3与TP53的相互作用至关重要,而且直接影响病毒的致病性。更有趣的是,研究者在其他小RNA病毒(如CV、EV71、SVA和PV)的VP3蛋白中也发现了该保守位点。当该位点突变为丙氨酸时,同样能够阻断这些病毒VP3蛋白诱导自噬和凋亡的功能。这表明,小RNA病毒可能采用了一种共性机制利用VP3蛋白调节其生命周期与致病性。这一发现不仅有助于深入理解小RNA病毒致病机制,还为广谱抗病毒药物及基因工程疫苗研发提供了新的靶点,为小RNA病毒引起的传染病防控和治疗提供新的思路。
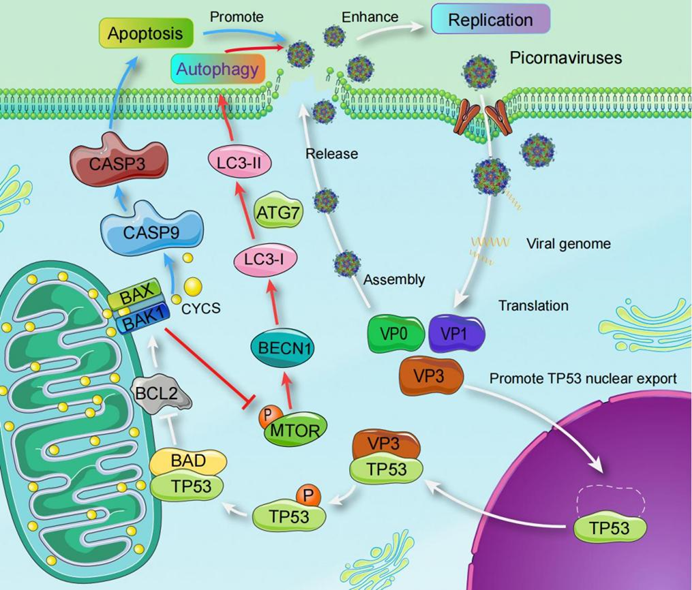
图1 小RNA病毒VP3调控自噬和凋亡促进病毒复制的机制示意图
中国农业科学院兰州兽医研究所郑海学研究员为本文通讯作者,毛箬青博士和朱紫祥研究员为本文共同第一作者。该研究得到国家重点研发计划、国家自然科学基金、国家生猪产业体系、中国农业科学院科学中心重大任务、甘肃省科技重大专项等项目资助。
文章链接:https://www.tandfonline.com/doi/full/10.1080/15548627.2024.2350270